| Q416★酸化還元反応に関する質問です。例えば、過マンガン酸カリウムなどは、酸化剤として教科書に書かれていて、より安定なMnO2やMn2+になりやすいと記載されています。この半反応式の右辺を見ると、失われた酸素は水や水酸化物イオンに変わっていることがわかります。一方で、有機化学のアルケンの開裂反応について調べたとき、過マンガン酸イオンが用いられていたのですが、ここでは酸素がアルケンを攻撃し、分裂するそれぞれに取り込まれる形で消費されていました。
そこで質問なのですが、(1)半反応式では、マンガンは水としか反応しない前提になっていますが、開裂反応の例では、水と反応したり、水が生成したりしていません。この矛盾はどうとらえたらいいでしょうか?(2)大学の簡単な教科書をみると、有機化学では反応の様子が電子の動きとして書かれているのですが、一般化学や無機化学の教科書では、そういった記載は見つかりませんでした。高校化学ででてくる無機化学の酸化還元反応が、どういう電子の動きをしているのか知りたいときは、どういった本やサイトを調べたらよいのでしょうか。
ご質問有難うございます。 (1)の質問について 酸化還元反応は三種類あると学校では学んでいるかと思います。 1.電子の授受を伴う酸化還元反応 2.酸素原子(分子)の授受を伴う酸化還元反応 3.水素原子(分子)の授受を伴う酸化還元反応 1.の酸化還元反応は、ダニエル電池や鉛電池、酸化還元滴定などで一般的に見られますが、反応式に電子(e−)が現れてくることから、酸化・還元反応に関係する物質のみで表現される「半反応式」と呼ばれる反応式で表します。例外も沢山存在しますが、一般的に金属イオンは水溶液中に存在することから、今回のような過マンガン酸カリウム(KMnO4)に含まれるマンガンイオンは7価であるために、より安定な4価の状態である二酸化マンガン(MnO2)や2価のMn2+に変化(還元)される半反応式においては、以下のように半反応式は表されます: 【酸性水溶液】 MnO4− + 8H+ + 5e− → Mn2+ + 4H2O 【中性・塩基性水溶液】 MnO4− + 2H2O + 3e− → MnO2 + 4OH− この半反応式において、もっとも重要な点は、「他の化学反応式と同様、反応前後の原子の数と電荷は等しい」ことです。上述の半反応式では、過マンガン酸イオンが2価あるいは4価に還元されるために、e−がいくつ必要かを考えます。その後、反応前後の原子数の過不足を補うためにH+やH2Oを用いられるのですが、よく見るとマンガンイオンの価数の変化に伴い、それまでマンガンイオンに結合していた酸素原子が放出され、周囲のH+やH2Oがこれを受け取っている形になっているために、H2OやOH−が生成していると表記されています。なお、1.の酸化還元反応においては、当然「電子の授受を伴う半反応式による酸化反応」も生じていることは忘れないでください。 では有機反応においてはどのように考えるべきでしょうか。酸性条件下におけるアルケンに対するKMnO4の反応を例に挙げてみましょう。 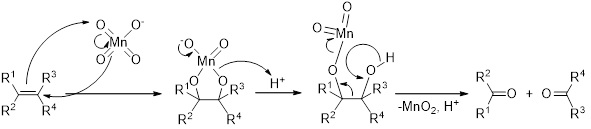 この反応においては、過マンガン酸イオン上の酸素原子が二つ、マンガンイオンからアルケンに移動していることがわかります。これは、2.酸素原子の授受に伴う酸化還元反応として考えることができ、過マンガン酸イオンは酸素原子を二つ放出することで還元され、安定な金属化合物の状態である二酸化マンガン(4価)へと変化します。一方で、アルケンは酸素原子を受け取ることで酸化され、その結果開裂していることから、「マンガンイオンの還元」と「アルケンの酸化」による酸化還元反応と考えることができます。 では、アルケンの開裂反応においては何故水と反応しないのでしょうか。上述のとおり、1.の電子の授受を伴う酸化還元反応においては、マンガンイオンの還元反応と同時に、「何らかの物質の酸化反応」が進行する必要があります。具体例を挙げるとシュウ酸の酸化反応、過酸化水素の酸化反応となりますが、アルケンには電子の授受を伴う酸化反応を進行させる能力がありません。そこで、2.の酸素原子の授受を伴う酸化還元反応が優先的に進行したと考えれば、特に矛盾は生じないかと思いますがいかがでしょうか。 (因みに上述の説明や反応式からは逸脱しますが、この反応は酸性条件下で行うため、「アルケンと水が反応して水素イオンと電子が生成する」と考えると半反応式は書けます) (2)高校化学学修範囲での無機化学における酸化還元反応での電子の動きを知るには? 無機化学においては、有機化学のように弧を描くような矢印で電子の動きを表しますが、無機化学では矢印を用いて表記することは稀です。インターネットで検索すると大学の講義で用いられているスライドが数多く掲載されていますので、どれを見ても参考になるかと思います。 私個人がお薦めしたいのは、 改訂版 フォトサイエンス化学図録(数研出版) です。酸化還元反応以外にも、高校化学で学ぶ内容をわかりやすく掲載していますので、休憩がてらに眺めるだけでもワクワクすると思います。 高2 (TN) 2024/07/11 |
 |